Zasady profilaktyki i nadzoru nad zakażeniami w zakładach opieki długoterminowej
27.11.2013
Ciąg dalszy dostępny po zalogowaniu dla osób związanych zawodowo z ochroną zdrowia.
Zaloguj się lub przejdź do portalu dla pacjentów.
Zaloguj się lub przejdź do portalu dla pacjentów.
Wybrane treści dla pacjenta
-
 Jersinioza Jersinioza to odzwierzęca choroba zakaźna powodowana przez bakterie z rodzaju Yersinia. Głównym rezerwuarem zwierzęcym szczepów Yersinia enterocolitica chorobotwórczych dla ludzi są świnie, dlatego zakażenie ma miejsce najczęściej po spożyciu skażonej żywności, w szczególności surowej lub półsurowej wieprzowiny lub podrobów wieprzowych.
Jersinioza Jersinioza to odzwierzęca choroba zakaźna powodowana przez bakterie z rodzaju Yersinia. Głównym rezerwuarem zwierzęcym szczepów Yersinia enterocolitica chorobotwórczych dla ludzi są świnie, dlatego zakażenie ma miejsce najczęściej po spożyciu skażonej żywności, w szczególności surowej lub półsurowej wieprzowiny lub podrobów wieprzowych. -
 Przeziębienie, grypa czy COVID-19? Pacjent może przebyć zakażenie koronawirusem z objawami kataru, grypa może mieć tak ciężki przebieg, że konieczna będzie hospitalizacja, a zakażenie wirusem RSV może skończyć się śmiercią – o infekcjach dróg oddechowych opowiada dr hab. Ernest Kuchar, specjalista chorób zakaźnych.
Przeziębienie, grypa czy COVID-19? Pacjent może przebyć zakażenie koronawirusem z objawami kataru, grypa może mieć tak ciężki przebieg, że konieczna będzie hospitalizacja, a zakażenie wirusem RSV może skończyć się śmiercią – o infekcjach dróg oddechowych opowiada dr hab. Ernest Kuchar, specjalista chorób zakaźnych. -
 Zatrucie pokarmowe Większość przypadków zatrucia pokarmowego ustępuje w ciągu paru dni bez konieczności zgłaszania się do lekarza. Podstawowe znaczenie ma nawadnianie doustne. Jeżeli zatrucie przebiega ciężko, lekarz może zdecydować o leczeniu szpitalnym i nawadnianiu dożylnym. W niektórych rodzajach zakażeń bakteryjnych przewodu pokarmowego lekarz może wyjątkowo zlecić antybiotyki.
Zatrucie pokarmowe Większość przypadków zatrucia pokarmowego ustępuje w ciągu paru dni bez konieczności zgłaszania się do lekarza. Podstawowe znaczenie ma nawadnianie doustne. Jeżeli zatrucie przebiega ciężko, lekarz może zdecydować o leczeniu szpitalnym i nawadnianiu dożylnym. W niektórych rodzajach zakażeń bakteryjnych przewodu pokarmowego lekarz może wyjątkowo zlecić antybiotyki. -
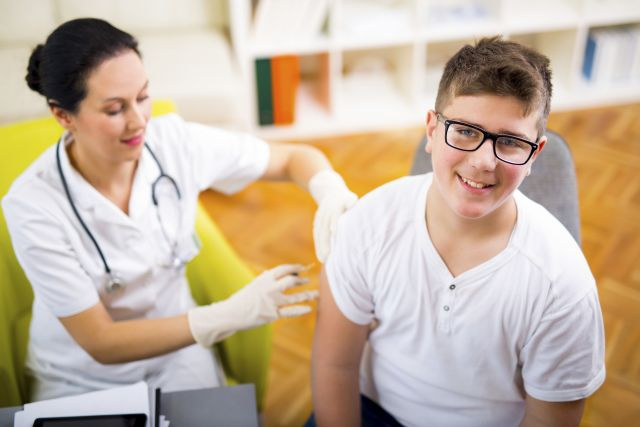
 Jak uchronić się przed grypą? Coroczne szczepienie zaleca się wszystkim osobom po ukończeniu 6. miesiąca życia, u których nie występują przeciwwskazania do szczepienia. Szczepienie nadal uważa się za najskuteczniejszą metodę zapobiegania zachorowaniom na grypę.
Jak uchronić się przed grypą? Coroczne szczepienie zaleca się wszystkim osobom po ukończeniu 6. miesiąca życia, u których nie występują przeciwwskazania do szczepienia. Szczepienie nadal uważa się za najskuteczniejszą metodę zapobiegania zachorowaniom na grypę. -
 Biegunka infekcyjna Biegunka infekcyjna jest chorobą spowodowaną przez czynnik zakaźny, która zwykle samoistnie, stopniowo ustępuje, nawet przed zasięgnięciem porady lekarza.
Biegunka infekcyjna Biegunka infekcyjna jest chorobą spowodowaną przez czynnik zakaźny, która zwykle samoistnie, stopniowo ustępuje, nawet przed zasięgnięciem porady lekarza. -
 Stolec – zmieniony wygląd Wygląd stolca jest związany z funkcjonowania układu pokarmowego. Prawidłowo powinien być dobrze uformowany, nie zawierać niestrawionych resztek pokarmu i dać się łatwo spuścić w toalecie. Zmieniony wygląd stolca może mieć różne przyczyny. Może być związany z dietą, przyjmowanymi lekami, a także chorobami układu pokarmowego
Stolec – zmieniony wygląd Wygląd stolca jest związany z funkcjonowania układu pokarmowego. Prawidłowo powinien być dobrze uformowany, nie zawierać niestrawionych resztek pokarmu i dać się łatwo spuścić w toalecie. Zmieniony wygląd stolca może mieć różne przyczyny. Może być związany z dietą, przyjmowanymi lekami, a także chorobami układu pokarmowego -
 Infekcje dróg oddechowych u dzieci U dzieci, szczególnie tych uczęszczających do żłobka, przedszkola lub posiadających starsze rodzeństwo w wieku przedszkolnym, rozpoznaje się średnio 8–10 infekcji dróg oddechowych w ciągu roku. Większość z nich to łagodne, samo-ograniczające się zakażenia górnych dróg oddechowych. Niektóre, np. zapalenie płuc lub zapalenie oskrzelików, mogą mieć jednak cięższy przebieg.
Infekcje dróg oddechowych u dzieci U dzieci, szczególnie tych uczęszczających do żłobka, przedszkola lub posiadających starsze rodzeństwo w wieku przedszkolnym, rozpoznaje się średnio 8–10 infekcji dróg oddechowych w ciągu roku. Większość z nich to łagodne, samo-ograniczające się zakażenia górnych dróg oddechowych. Niektóre, np. zapalenie płuc lub zapalenie oskrzelików, mogą mieć jednak cięższy przebieg. -
 Zakażenia meningokokowe, sepsa meningokokowa Inwazyjna choroba meningokokowa jest najczęstszą postacią zakażeń meningokokowych – ciężką, gwałtownie postępującą chorobą bakteryjną wywołaną przez wtargnięcie dwoinek zapalenia opon do prawidłowo jałowych miejsc organizmu, takich jak krew i ośrodkowy układ nerwowy.
Zakażenia meningokokowe, sepsa meningokokowa Inwazyjna choroba meningokokowa jest najczęstszą postacią zakażeń meningokokowych – ciężką, gwałtownie postępującą chorobą bakteryjną wywołaną przez wtargnięcie dwoinek zapalenia opon do prawidłowo jałowych miejsc organizmu, takich jak krew i ośrodkowy układ nerwowy. -
 Szczepienie przeciwko grypie – niepożądane odczyny poszczepienne (NOP) Większość zdarzeń niepożądanych po szczepieniu przeciwko grypie to reakcje o łagodnym przebiegu, które zwykle ustępują w ciągu 1–2 dni. Ciężkie zdarzenia niepożądane po szczepieniu przeciwko grypie występują bardzo rzadko. Bardzo rzadko po szczepieniu przeciwko grypie u osób uczulonych na składniki szczepionki mogą wystąpić reakcje alergiczne, w tym ciężkie z wstrząsem włącznie.
Szczepienie przeciwko grypie – niepożądane odczyny poszczepienne (NOP) Większość zdarzeń niepożądanych po szczepieniu przeciwko grypie to reakcje o łagodnym przebiegu, które zwykle ustępują w ciągu 1–2 dni. Ciężkie zdarzenia niepożądane po szczepieniu przeciwko grypie występują bardzo rzadko. Bardzo rzadko po szczepieniu przeciwko grypie u osób uczulonych na składniki szczepionki mogą wystąpić reakcje alergiczne, w tym ciężkie z wstrząsem włącznie. -
 Test combo – grypa, COVID-19, RSV Test combo to test diagnostyczny do samodzielnego wykonania, za pomocą którego można potwierdzić zakażenie wirusami grypy, SARS-CoV-2 (powodującym COVID-19) oraz RSV. Test combo można kupić w aptece za około 20 zł. Najbardziej wiarygodny wynik testu uzyskuje się na początku choroby
Test combo – grypa, COVID-19, RSV Test combo to test diagnostyczny do samodzielnego wykonania, za pomocą którego można potwierdzić zakażenie wirusami grypy, SARS-CoV-2 (powodującym COVID-19) oraz RSV. Test combo można kupić w aptece za około 20 zł. Najbardziej wiarygodny wynik testu uzyskuje się na początku choroby